Prácticas de Laboratorio
Fechas:
Neón A: jueves 5 de enero de 2017
Neón B: martes 3 de enero de 2017
Fechas:
Neón A: jueves 5 de enero de 2017
Neón B: martes 3 de enero de 2017
¡Bienvenidos al segundo quimestre,
queridos Neones!
TETRIS
Diviértete con este juego y aprende la ubicación de los elementos en la tabla periódica. Recuerda registrarte y enviar tu datos junto con una captura de pantalla de los resultados
Diviértete con este juego y aprende la ubicación de los elementos en la tabla periódica. Recuerda registrarte y enviar tu datos junto con una captura de pantalla de los resultados
http://www.quimitris.com/
En el siguiente vínculo podrán leer una breve pero precisa historia de la evolución de la tabla periódica
http://www.lenntech.es/periodica/historia/historia-de-la-tabla-periodica.htm
http://www.lenntech.es/periodica/historia/historia-de-la-tabla-periodica.htm
Práctica de Laboratorio del lunes 20 de febrero (10 mo. B) y martes 21 de febrero (10 mo. "A")
Recuerden revisar las rúbricas de las prácticas de laboratorio (página principal del blog) para que puedan preparar adecuadamente su desempeño en en el laboratorio
Recuerden revisar las rúbricas de las prácticas de laboratorio (página principal del blog) para que puedan preparar adecuadamente su desempeño en en el laboratorio
En el siguiente video podrán observar la reacción de una sal de un halógeno (yodo) el KI con nitrato de plomo (II) Pb(NO3)2 :
Pulsando el siguiente botón obtendrás información de la prueba para la identificación de halógenos con nitrato de plata:
Proyecto de unidad:
Diseño de juego didáctico sobre la tabla periódica y las propiedades de los elementos
La idea de este proyecto es que los estudiantes de décimo diseñen un juego mediante el cual puedan aprenderse de manera sencilla las propiedades de los elementos de la Tabla Periódica. En el siguiente archivo PDF podrán encontrar algunos ejemplos interesantes.
Más abajo hay información (videos) con la cual deben hacerse los juegos: Radio atómico, afinidad electrónica, energía de ionización.
Diseño de juego didáctico sobre la tabla periódica y las propiedades de los elementos
La idea de este proyecto es que los estudiantes de décimo diseñen un juego mediante el cual puedan aprenderse de manera sencilla las propiedades de los elementos de la Tabla Periódica. En el siguiente archivo PDF podrán encontrar algunos ejemplos interesantes.
Más abajo hay información (videos) con la cual deben hacerse los juegos: Radio atómico, afinidad electrónica, energía de ionización.
| juegos.pdf | |
| File Size: | 219 kb |
| File Type: | |
En los siguientes videos se explica de manera bastante clara las principales propiedades de los elementos relacionándolas con la ubicación de los mismos en la tabla periódica
Repasando:
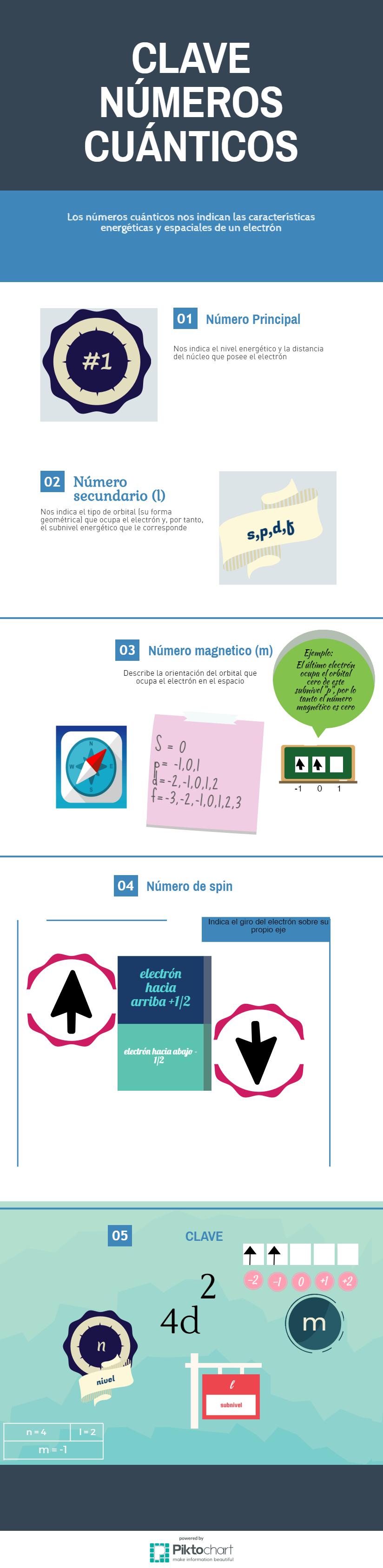
Clave para números cuánticos.
Clave para números cuánticos.
Segunda unidad
¡Vamos al teatro!
En esta unidad vamos a hacer una representación teatral del tema "Enlaces químicos"
En esta unidad vamos a hacer una representación teatral del tema "Enlaces químicos"
Proyecto de Unidad:
El proyecto para esta unidad será hacer un cartel digital didáctico sobre los enlaces químicos. La idea es que el cartel sirva para enseñar a otros estudiantes cómo estudiar y aprender este interesante y útil tema de la química.
El proyecto para esta unidad será hacer un cartel digital didáctico sobre los enlaces químicos. La idea es que el cartel sirva para enseñar a otros estudiantes cómo estudiar y aprender este interesante y útil tema de la química.
Juego en clases
http://www.testeando.es/test.asp?idA=43&idT=hzkchkio
En clases formaremos grupos para jugar esta emocionante trivia sobre los tipos de enlaces
http://www.testeando.es/test.asp?idA=43&idT=hzkchkio
En clases formaremos grupos para jugar esta emocionante trivia sobre los tipos de enlaces
Simulación PHET (University of Colorado)
https://phet.colorado.edu/sims/html/atomic-interactions/latest/atomic-interactions_es.html
En este simulador te permitirá observar cómo influye el tamaño y tipo de átomo en la tendencia a formar enlaces químicos
https://phet.colorado.edu/sims/html/atomic-interactions/latest/atomic-interactions_es.html
En este simulador te permitirá observar cómo influye el tamaño y tipo de átomo en la tendencia a formar enlaces químicos
| rúbrica_dramatización.pdf | |
| File Size: | 96 kb |
| File Type: | |
Unidad 6
Deber (fecha de entrega lunes 22/05 (10B) martes 23/05 (10A)
Investigar:
Deber (fecha de entrega lunes 22/05 (10B) martes 23/05 (10A)
Investigar:
- Concepto de pH (Explicar)
- Concepto de POH (Explicar)
- Cálculos relativos a pH y pOH (indicar por lo menos dos ejemplos de problemas resueltos)
| rúbrica_lapbook_10_mo..docx | |
| File Size: | 19 kb |
| File Type: | docx |
Cuestionario de Examen Quimestral
Propiedades periódicas: de las siguientes propiedades responda:
Propiedades: Energía de ionización/ Afinidad Electrónica
a) Explicación
b) Forma de variación en la tabla periódica y justificación
Enlaces químicos:
Una molécula está conformada por dos elementos no metales en la proporción 2:1 (dos átomos de un elemento por cada átomo del otro)
Posible estructura de la molécula: Respuesta: Ej. H2O
Tipos de enlaces y cómo se forman: Respuesta: Covalente, se forman al compartirse electrones de la última capa
Propiedades de la sustancia (justifique):
Punto
de ebullición
Punto
de fusión
Conductividad
Respuestas (para enlace covalente y enlace iónico)Compuestos Iónicos
- Sólidos cristalinos (hechos de iones)
- Altos Puntos de Ebullición y Fusión
- Conductores de la Electricidad en estado fundido
- Muchos son soluble en agua, pero no en líquido no polar
- Gases, líquidos, o sólidos (hechos de moléculas)
- Bajos Puntos de Ebullición y Fusión
- Pobres conductores eléctricos en todas las fases
- Muchos son solubles en líquidos no polares pero no en agua
Qué tipo de enlace debería tener una sustancia sólida conductora de electricidad. Dé ejemplo. Justifique su respuesta
pH
Explique cómo funciona el siguiente buffer o tampón ante añadidos de ácidos (8 puntos).
Ácido carbónico = bicarbonato + protón
H2CO3 = HCO3 + H+
Respuesta: ante el agregado de ácidos (H) el bicarbonato los captura para regenerar el ácido carbónico y ante el agregado de bases (OH) el protón lo captura para formar agua